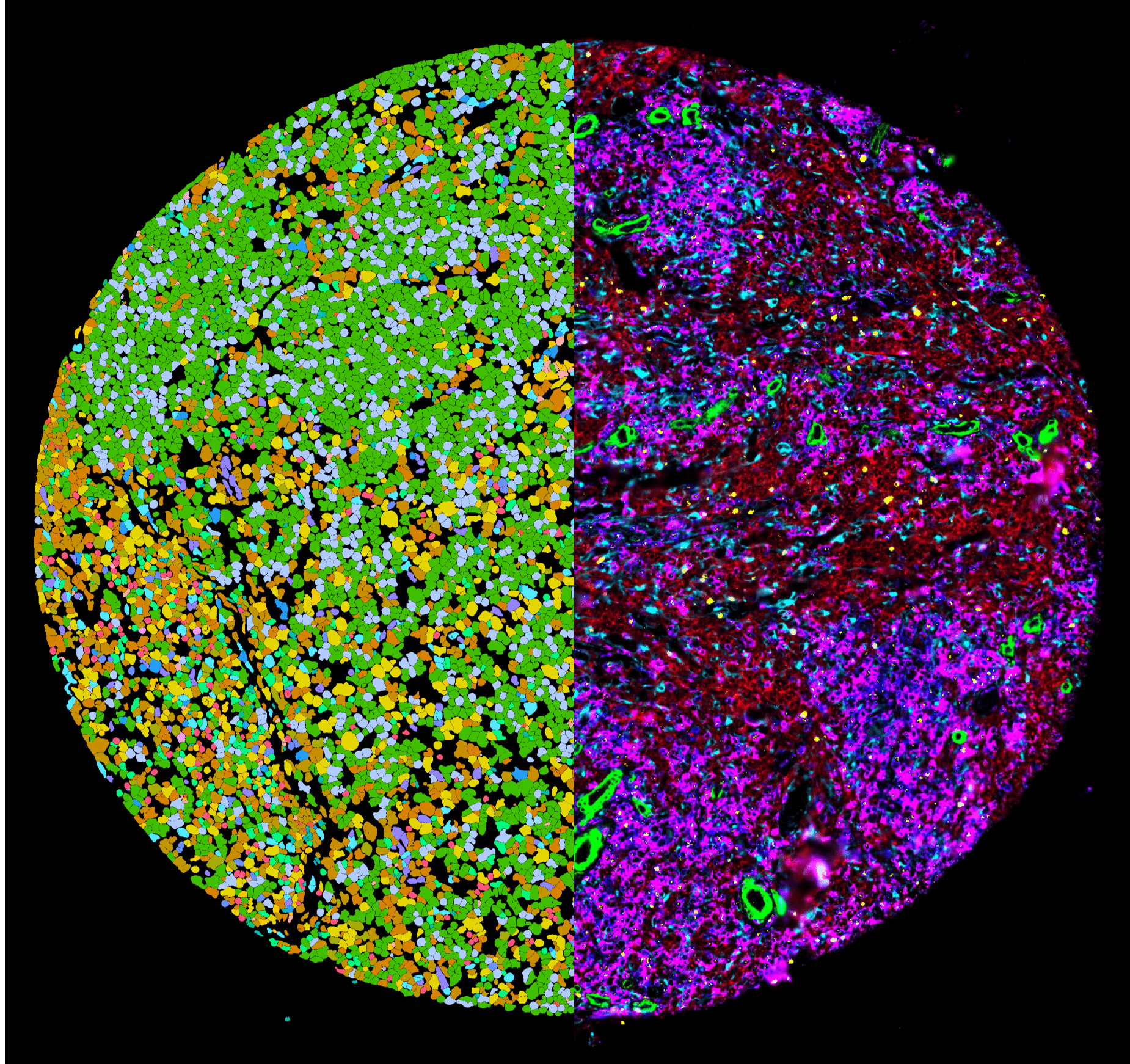Ziel des INTeRCePT-Projekts ist es, personalisierte Therapiestrategien für Patient:innen mit Lymphdrüsenkrebs zu entwickeln, indem tumor- und immunologische Veränderungen während des gesamten Krankheitsverlaufs systematisch analysiert werden. Durch die Kombination longitudinaler Probenanalysen mit modernen Computermodellen sollen Therapieansprechen frühzeitig vorhergesagt und Behandlungen gezielt angepasst werden, um Wirksamkeit zu erhöhen, Nebenwirkungen zu reduzieren und aggressive Verläufe besser zu kontrollieren.
Im Zurich Precision Oncology Consortium INTeRCePT entwickeln Ärztinnen, Ärzte und Forschende neue Ansätze für eine dynamische Präzisionsonkologie.
Über 1’000 Tumor- und Blutproben werden longitudinal analysiert – also vor und insbesondere früh während der Therapie. In Kombination mit modernen Computermodellen entsteht ein individuelles Risikoprofil, das frühzeitig zeigt, ob eine Behandlung wirkt.
Im Unterschied zu klassischen Studien, die oft einzelne Zeitpunkte betrachten, analysiert INTeRCePT 3.0 den gesamten Krankheitsverlauf. Dadurch können Therapien früher angepasst und gezielter eingesetzt werden.
Technologischer Ansatz
INTeRCePT 3.0 kombiniert longitudinale und multimodale Analysen, um Tumor- und Immunveränderungen präzise zu erfassen und in prädiktive Modelle zu überführen:
Analyse von über 1’000 Tumor- und Blutproben
Hochauflösende Einzelzell- und Multi-Omics-Verfahren
Liquid Biopsies zur Erfassung zirkulierender Tumor-DNA (ctDNA)
Hochdimensionale Immunprofilierung
Entwicklung quantitativer Modelle und Einsatz von Machine Learning
“Wir versuchen zum frühestmöglichen Zeitpunkt den Verlauf von Lymphompatient:innen vorherzusagen. Dabei nutzen wir hochauflösende Analysen vor und direkt nach der Therapie. Wir erhoffen uns von den Versuchen einen wichtigen Schritt hin zur personalisierten Krebstherapie.”
Prof. Dr. med. Thorsten Zenz - Klinik für Medizinische Onkologie und Hämatologie, USZ

Projektteam

Prof. Dr. med. Thorsten Zenz, Universitätsspital Zürich, Klinik für Medizinische Onkologie und Hämatologie , thorsten.zenz@usz.ch

Prof. Dr. Burkhard Becher, Universität Zürich, Institut für Experimentelle Immunologie, becher@immunology.uzh.ch

Prof. Dr. Niko Beerenwinkel, ETH Zürich, Institute for Biomedical Engineering, niko.beerenwinkel@bsse.ethz.ch

Prof. Dr. Valentina Boeva, ETH Zürich, Department of Computer Science, valentina.boeva@inf.ethz.ch

Dr. med. Marco M Bühler, Universitätsspital Zürich, Institut für Pathologie und Molekularpathologie, marcomatteo.buehler@usz.ch

Prof. Dr. Wolfgang Huber, EMBL, wolfgang.huber@embl.org

Prof. Dr. Andreas Moor, ETH Zürich, Department of Biosystems Science and Engineering, andreas.moor@bsse.ethz.ch

Prof. Dr. Virginie Uhlmann, Universität Zürich, Institut für Molekulare Biologie, virginie.uhlmann@mls.uzh.ch
Untersuchte Krebserkrankungen
Lymphome
Fördervolumen
CHF 4’050’000
Gefördert von
CCCZ, The LOOP Zurich, Tumor Profiler Center
Laufzeit
2026-2030
Weitere Projekte
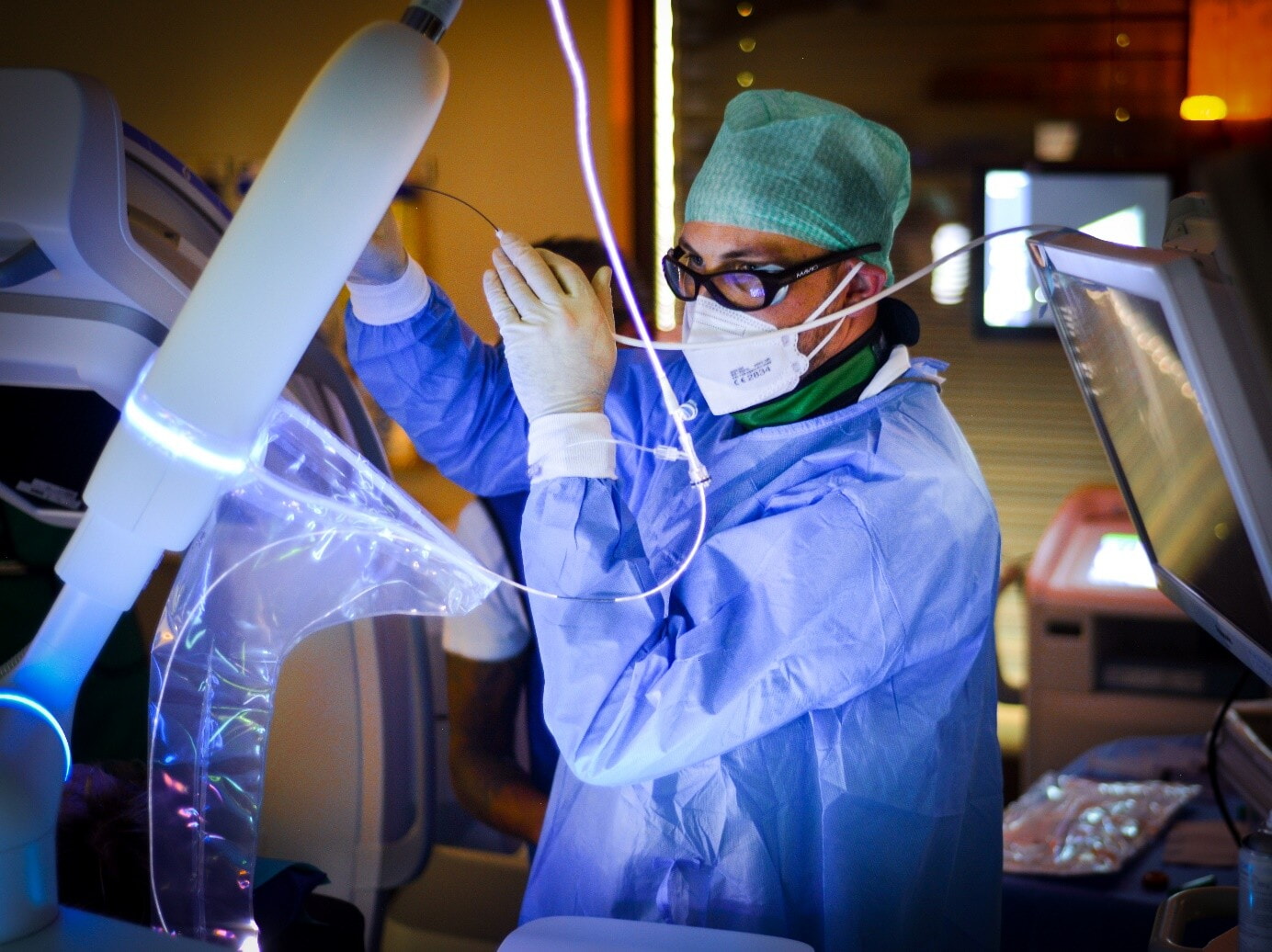
CCCZ Klinische Studie
BRAVE-Lung
Robotergestützte bronchoskopische Radiofrequenzablation bei Lungenkrebs im Frühstadium - eine neuartige Krebstherapie
CCCZ Leuchtturmprojekte
Interdisziplinäre Forschungsteams übertragen Erkenntnisse aus der Grundlagenforschung in die klinische Anwendung und entwickeln neue Behandlungskonzepte gegen Krebs.